Halk Sağlığı Genel Müdürlüğü’nden tetanoz difteri aşılarının geri çekilmesine ilişkin açıklama
Sağlık Bakanlığı Halk Sağlığı Genel Müdürlüğü, bir firma hakkında tetanoz difteri aşılarının toplanmasını gerektirecek herhangi bir olumsuz etkinin yapılmadığını, kurul kararıyla ilgili serilere bazı süreçlere bağlı olarak geri çekilme uygulandığını bildirdi. son kontrolde eksik olduğu tespit edildi.
Halk Sağlığı Genel Müdürlüğü’nden yapılan açıklamada, kullanıma sunulan her aşının Türkiye İlaç ve Tıbbi Cihaz Kurumu (TİTCK) Ulusal Referans Laboratuvarlarında analiz edildiği ve aşılanıncaya kadar Aşı Takip Sistemi ile takip edildiği belirtildi. etkinliğinden ve güvenliğinden emin olduktan sonra bireylere uygulanır.
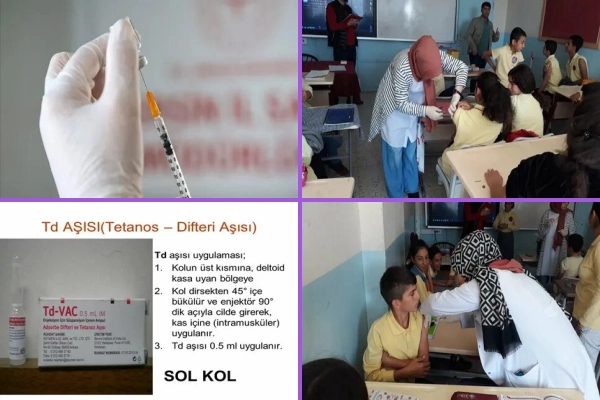
TİTCK tarafından geri çekilme süreci başlatılan “Tetadif 0,5 ml IM Injectable Suspension” adlı çalışmanın, yetişkin tetanoz difteri aşısı ve teknoloji transfer desteği sağlanarak ilk aşamadan Türkiye’de üretilecek ilk aşı olduğu belirtildi.
TİTCK tarafından üretimin her sürecinin düzenli bir şekilde takip edildiğinin belirtildiği açıklamada, şunlar kaydedildi:
“Bu noktada aşının geri çağrılmasını gerektirecek herhangi bir yan etki bildirilmedi ancak son kontrolde eksik bulunan bazı işlemlerden dolayı kurul kararına göre seri geri çekildi. Raf ömrü Yeni üretilen aşıların yüzde 30’u özel kurallara uyularak kademeli olarak 3 yıla kadar uzatılıyor. Söz konusu aşının raf ömrü de bu türden. “Bir süre sonunda 2 yıldan 3 yıla çıkarıldı. Söz konusu aşının son kullanma tarihini uzatma süreci değil bu. Yeterince kontrol edilmiş ve kullanıma uygun yeterli aşı stoğumuz var. Bu açıdan rastgele problemler söz konusu değil.”









